こんにちは、「しがない化学科生達のブログ」編集のこたつです。
最近は院試の勉強で忙しくしているのですが、勉強中ふと疑問に思って調べたことがあったので共有させてください。
化合物の詳細な構造を知りるために行うNMRですが、スペクトルを読み解くにあたって、積分値、化学シフト、多重度の情報が鍵となります。
今回は3つ目の多重度に関して、タイトルにもあります通り、HNMRでなぜ等価なプロトンがカップリングしないのかについて話していきたいと思います。
その前に少しカップリングについて簡単に復習をしましょう。早く結論が知りたいという方は、本題へ飛んでいただいて構いません。
以下の文中では、いわゆる上向きスピンをα、下向きスピンをβと表記してます。
復習
多重度とは、隣接水素の数によってピークが何本に分裂するかを表す数字です。
これは、注目している水素のスピンに対し、隣接水素のスピンが平行か反平行かでエネルギー準位が変わるためです。
有機化学もしくは分析化学で、多重度は隣接した炭素上の水素の数+1となる、いわゆるn+1の法則を習ったと思います。
例えば、2つの隣接水素があったときに、それらのスピンの組み合わせはαα、αβ、βα、ββとなりますが、αβとβαは与える影響が一緒なのでピークが重なって、結局3本のピークが1:2:1の強度で現れることになります。
3つの隣接水素の場合も同様で、αスピンの数が3から0までの4通りあるので、四本のピークが生成されるといったように、n+1本のピークが観測されます。
さて、今回の疑問は隣接炭素上の水素でなく、同じ炭素に乗った等価な水素間でも同様の状況が成り立つのではというものです。
例えば、メタンの一つの水素に着目した場合、残り3つの水素のスピンがααα、ααβ、αββ、βββ、の可能性がありますから(同じ数のスピンを含む組は省略しています)、ピークは4分裂するのではないかという話です。
本題
結論から言うと、等価な水素間でもカップリングはするけれど、カップリングを考慮する前と後でエネルギー準位はスライドするだけなので、観測される遷移はカップリングしないとしたときと同じ、ということになります。
ここでは2個の等価な水素がある分子を考えましょう。(例えばCH2D2を想像してください)
2つのプロトンのスピンの組はαα、αβ、βα、ββの4通りです。これは正しいのですが、カップリングの挙動を表すときにはαβとβαは重ねわせて
A={1 \over \sqrt 2}( \alpha \beta+\beta\alpha)B={1 \over \sqrt 2}( \alpha \beta-\beta\alpha)としたほうがわかりやすいです。
なぜなら、実はカップリングによってαα、A、ββはどれもエネルギー準位がhJ/4だけ上昇し、BだけhJ3/4だけ下がるからです。ここでhはプランク定数で、Jはカップリングの強さを表す比例定数です。
図にすると以下のようになります。
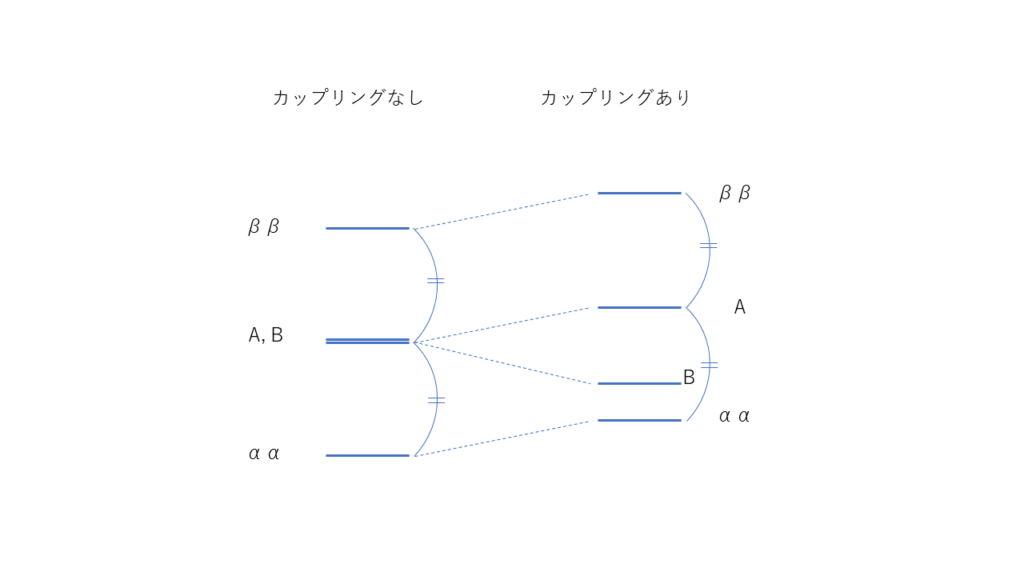
さらに、遷移が起こるのはαα-A間、A-ββ間のみで、エネルギーのスライドしていないBは遷移に関与することはできません。
なぜこのようになるかは少々難しい議論が必要なのでここでは割愛します。詳しく知りたい方はアトキンス物理化学下第10版の616ページをご参照ください。
多くの有機化学の教科書では、等価な水素はカップリングしないと記述されていることが多く、誤解をしてしまう方が多いのですが、こういうカラクリでした。
改めて結論を言うと、等価な水素もカップリングはするけれど、しないと考えてもNMRのチャートを読むのには全く問題ない、というのが答えになります。
でも、ちょっと深堀りしようとすると、すぐにおかしいなと気づくようなことなので、有機の教科書にも、ちょこっと書いてくれたら親切だな~と思いました。